실험동물운용팀
- Home
- 연구소
- 암연구코어센터
- 실험동물운용팀

AAALAC 인증 기관으로서의 신뢰도를 바탕으로, 차세대 암치료법 개발을 위한 이행성 연구 인프라를 목표로 하며, 표준화/자동화 된 사육관리 시스템 및 조직 병리 시스템을 기반으로 실험동물 모델을 이용한 전임상 연구 수행을 지원
실험동물 관리
- 사육관리의 표준화
- 실험동물 품질 관리
- 수의학적 관리
- 실험동물 자원 관리
암동물모델 제작
- 유전자변형 마우스 제작
- 이종이식 모델 제작
동물실험 인프라 제공
- AAALAC 인증 동물실험시설
- 동물실험시설, 연구장비 지원
- 유전자재조합물질, 병원체 및 발암물질 적용모델 연구지원
- 방사선조사 동물모델 연구지원
조직병리시스템
- 조직병리
- 면역염색
- 혈액생화학 분석
연구병리 판독
- 염색 슬라이드 병리 분석
연구자 교육
- 실험동물 사용 및 관리에 관한 이론 교육
- 이용자교육
- 동물실험 기법교육

동물실험지원
- 실험동물 관리 : 설치류, 국제표준가이드, 수의학적 관리
- 동물모델 지원 : 형질전환동물(GEM), 종양 이식 마우스모델
- 인프라지원 : 유전자재조합 병원체 발암물질 적용 모델, 방사선조사 모델
- 시설 및 장비/소프트웨어 : SPF(Specific Pathogen Free) 사육시설, 자동공조, 보안시스템, 환경모니터링, GEM (genetic engineering mouse) room, 마우스배아미세주입장치, ABSL2 시설, 세포 및 동물용 방사선 조사기 XenX
조직병리분석
- 조직병리 : 병리조직 파라핀블록 제작, 슬라이드절편 제작 및 H&E 염색, 동결절편 제작 및 염색 실시
- 면역염색 : 면역조직화학방식을 사용한 항체염색, 슬라이드 자동스캔 및 분석
- 혈액분석 : 혈액성분 생화학분석-GOT, GPT, …
- 연구병리판독 : 염색슬라이드 병리분석
- 시설 및 장비/소프트웨어 : 조직처리기 (Histocore Peral), 조직포매기 (EC350), 파라핀절편기 (HM340E-1), 자동염색기 (LEICA5010), Cryotome 동결절편기 (HM525), Fully Automatic IHC&ISH Staining, System(Discovery XT, Ventana), Automated Quantitative Pathology, Automatic Chemistry Analyzer(DryCHEM3500i)
실험동물보존
- 수정란 동결보존
- 시설 및 장비/소프트웨어 : 초자화동결보관 (MVE Cryosystem)
연락처
- 총괄지원 : 이호, ho25lee@ncc.re.kr, 031-920-2274
- 동물실험지원 : 김보라, mouse@ncc.re.kr, 031-920-2111
- 조직병리 분석 : 박미선, parkms@ncc.re.kr, 031-920-2113
실험동물모델 인프라
실험동물실 이용자 교육
- 교육 대상 : 실험동물실을 이용하고자 하는 연구자
- 교육일정 : 매월 1회(정기)
- 교육 내용(실험동물실 투어 포함) : 실험동물윤리교육, 실험동물실 소개, 출입절차 설명, IACUC 심의서류 접수안내, 인도적인 동물실험방법, 실험동물 반입절차, 기타 유의사항
- 신청 절차 : 이용자교육신청서 및 출입권한신청서 작성 제출
- 이용자교육을 이수한 후 출입증 인증 절차를 거쳐 출입이 가능(외부연구자의 경우, 서약서 별도 작성)
동물실험을 위한 3R 원칙
- Reduction: 과학적인 통계기법을 사용하고 중복실험을 감소시켜 희생동물 수를 줄임
- Replacement: 대체수단을 강구하여 동물실험을 줄임
- Refinement: 과학적이며 인도적인 실험방법을 이용하여 동물의 스트레스와 고통을 최소화
- 동물실험을 실시하는 연구자는 3R 원칙하에 연구를 수행해야 함.
- 3R에 입각한 동물실험은 실험동물에 대한 인도적 측면 뿐만 아니라 실험 외 요인을 최소화 함으로써 과학적인 결론을 도출할 수 있으므로 필수적으로 검토되어야 함.
현황
- 실험동물사육실은 면적 1,824m3의 규모로 최대 3만 마리의 실험동물을 동시에 사육 가능하며 연구동 6층에 위치하여,
연구소의 다른 층과 분리된 공조 설비와 보안 시스템으로 관리되고 있음 - 설치류 전문 SPF (특정 병원성미생물 부재, Specific Pathogen Free)연구시설로, 개별공조케이지(IVC) 시스템으로
각 실험에 대한 독립성과 청정성 유지 - AAALAC (국제실험동물인증협회) 인증 실험동물시설
| 층별 | 면적(㎡) | 용도 |
|---|---|---|
| 6F | 1,824 | - 설치류 사육 및 실험 시설 - IVC Rack (65 set) : 최대 3만 여수 사육 가능 |
| 1F | 140 | - 연구지원 : 조직제작, 혈액분석, 동결보존, 미생물검사 |
| 7F | 1,566 | - 공조설비, 부검실 |
| B1F / B3F | 500 | - 지하창고, 사체처리창고, 저온창고 Boiler, 전기/steam control. |
시설도면도
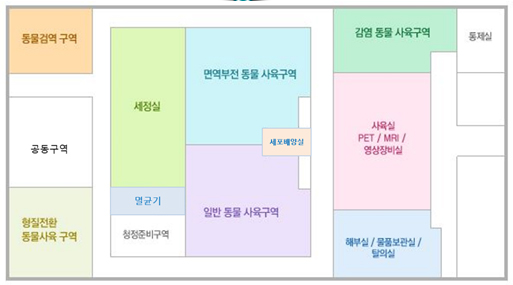
실험동물 사육관리 및 사용자 안전관리
- 설치류용 개별환기사육장비 (IVC)에 기반한 실험동물 품질유지
- 케이지 바코드 시스템 : 해당 PI의 이름 및 승인번호, 동물정보 입력 관리
- 매일 전문 사육관리자들에의한 실험동물의 상태 관찰 및 기록
- 분기별 검사와 검역
- 일회용 멸균 보호복 사용 및 감염성폐기물 관리

실험동물 검역 및 미생물모니터링
- 정기적인 미생물 모니터링을 통해 SPF 실험동물의 청정도를 감시하고 있으며, 월 1회 실시되는 환경모니터링을 통해 사육환경을 관리함
- 외부 기관에서 반입할 경우는 해당 외부기관의 ‘미생물모니터링자료’, ‘시설설명서’, ‘수의사 반출동의서’ 등을 참고하여 IACUC에서 live-stock의 반입 가부를 결정하며, IACUC 특별 승인 후 본 기관에서 미생물모니터링을 실시하여 검역한 후 반입함
최종 수정일 : 2019.08.16
실험동물 시료분석
조직병리 (위치 : 연구소 1층)
- 암 조직 등 원하는 병변을 고정 처리후, 파라핀을 침투시킨 파라핀블록을 제작하거나, 동결조직블록을 제작하여 얇은 절편슬라이드로 제작하고, 필요한 염색을 실시하여 병변을 확인하고 분석할 수 있도록 시료를 처리함
- 자동조직처리, 자동염색장비 도입 운영중

면역염색
- 암 조직 등 원하는 병변을 절편으로 제작하여, 항원복구 및 항체처리 과정을 통해 면역반응을 이용한 염색을 실시하고, 원하는 항원과 항체의 결합을 발색제 혹은 형광으로 확인할 수 있도록 처리함.
- 보유장비: 전자동면역염색장비 (Discovery XT, VENTANA)
자동다중스캔분석
- 염색된 절편을 스캔하여 전자슬라이드로 제작하고, 구획을 분류하여 정량분석을 실시함.
- Automated Quantitative Pathology Imaging Scan System (Vectra Polaris, Perkin Elmer)
- Automated Quantitative Pathology Imaging Analysis Program (InForm, Perkin Elmer)

최종 수정일 : 2019.08.16

동물실험윤리위원회(IACUC)
Institutional Animal Care and Use Committee
위원회의 권한
기관장 직속의 독립적 법정위원회 (근거: 동물보호법, 실험동물에 관한 법률)위원회의 기능
- 동물실험계획의 윤리적, 과학적 타당성에 대한 심의 및 승인
- 승인 후 점검 (PAM:Post Approval Monitoring)
- 동물실험시설의 운영실태의 확인 및 평가
- 실험동물의 사용 및 관리에 관한 프로그램에 대한 평가
동물실험 수행절차
- 법정교육 이수
- 실험동물의 사용 및 관리에 관한 교육
- LMO 교육
- 방사선교육(기본/직장)
- 이용자교육(NCC)
- 동물실험 계획서 제출
- 심의 및 IACUC 승인
- 필요시 위원회 연계(IRB,IBC)
- 생물학적 위해물질 사전보고(식약청)
- 동물 구입&반입
- LMO수입신고
- 검역 및 순화
- 동물실험 수행
- 처치 후 관리
- 인도적 종료시점 준수
- 안락사
- 결과분석, 실험종료
- 종료보고서 IACUC 제출
- 법정교육 이수